Cụ thể, nhà khoa học Nga Denis Rebrikov dự định sẽ chỉnh sửa gene phôi cho 5 cặp vợ chồng người Nga để giúp con cái họ thoát khỏi bệnh điếc bẩm sinh. Đây là dự án tiếp theo đang được dư luận quan tâm sau khi nhà khoa học Trung Quốc, He Jiankui công bố đã chỉnh sửa gene cho các bé gái, giúp các em không bị nhiễm HIV từ người cha truyền cho.
Nếu dự án trên được thực hiện, thì Denis Rebrikov có thể là người tiếp theo được dư luận quan tâm. Theo ông Denis Rebrikov, đây là việc cần làm nhiều vì lý do, nhưng cái chính vẫn là giúp 5 gia đình ngăn chặn truyền bệnh điếc cho con do đột biến gene GJB2 gây ra.

Cũng theo Rebrikov, bằng cách chỉnh sửa khuyết khiếm gene GJB2 trong phôi khi thụ thai sẽ khắc phục được căn bệnh này. Nhưng không giống như nhà khoa học ở Trung Quốc, Rebrikov làm có bài bản hơn, trước tiên là tiếp cận với Chính phủ Nga để được cấp phép sau đó mới bắt tay vào thực hiện dự án.
Liên quan đến bệnh điếc bẩm sinh, đầu tháng 7/2019, Đại học Y khoa Harvard và BV Nhi đồng Boston (Mỹ) đã công bố kết quả nghiên cứu vừa hoàn thành, hy vọng có thể ngăn ngừa bệnh điếc di truyền bằng chỉnh sửa gene. Thử nghiệm ở chuột bị mất thính lực di truyền đã thành công mà không để lại bất kỳ tác dụng phụ ngoài mong muốn. Chuột được cứu vãn thính giác trong nghiên cứu có tên Beethoven (lấy theo tên nhà soạn nhạc Ludwig van Beethoven, người bị điếc nhưng nguyên nhân hiện vẫn chỉ là giả định). Nó được điều trị một đột biến gene gây mất thính lực tiến triển giống như ở người, khiến người bệnh dễ bị điếc sâu vào giữa tuổi 20. Bằng công cụ CRISPR-Cas9, các nhà khoa học vô hiệu hóa một cách có chọn lọc bản sao khiếm khuyết của gene có tên Tmc1.
Ở chuột Beethoven lỗi gây điếc thể hiện không chính xác trong chuỗi ADN của gene Tmc1, chữ A thay bằng T, lỗi duy nhất cho thấy sự khác biệt giữa thính giác bình thường và điếc. Vô hiệu hóa hoặc làm “câm” bản sao đột biến của gene Tmc1 sẽ đủ để bảo vệ thính giác của động vật, nhưng làm thế nào để có thể thực hiện được điều này mà không vô tình làm mất chức năng của gene khỏe mạnh là câu hỏi đặt ra.
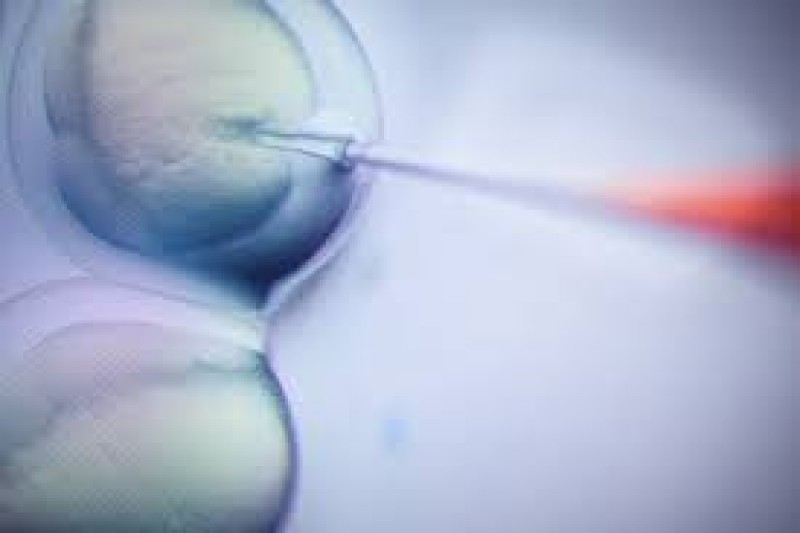
Để vượt qua thách thức này, nhóm nghiên cứu đã căn chỉnh công cụ ban đầu được phát triển bởi Keith Joung, giáo sư bệnh học và GS Ben Kleinstiver ở Đại học Y khoa Harvard, sử dụng enzyme Cas9 biến đổi có nguồn gốc từ Staphylococcus aureus thay vì Cas9 tiêu chuẩn có nguồn gốc từ vi khuẩn Streptococcus pyogenes. Nhằm tăng độ chính xác cho hệ thống mới, các nhà khoa học đã kết hợp hai cấp độ nhận dạng - gRNA để xác định gene mục tiêu và Cas9 được sửa đổi xác định đột biến AND cụ thể ở chuột Beethoven. Việc sử dụng hai hình thức nhận dạng trên giúp cắt chính xác và chọn lọc bản sao bất thường, chỉ nhắm vào bản sao bất thường của gene đó chứ không ảnh hưởng đến gene khỏe mạnh.
Hứa hẹn điều trị 15 dạng điếc di truyền
Với công cụ phân biệt chính xác giữa ADN đột biến và ADN bình thường trong các bản sao của Tmc1, các nhà khoa học đã đạt ngưỡng chính xác 99% các phân tử cắt giảm trong bản sao khiếm khuyết của gene. Phân tích ADN cho thấy, hoạt động chỉnh sửa chỉ xảy ra ở các tế bào tai trong của chuột bị khiếm khuyết Beethoven còn chuột được điều trị mà không có đột biến thì không có tác dụng phụ, các phản ứng thính giác không thay đổi.
Riêng chuột Beethoven bị điếc hoàn toàn sau 6 tháng tuổi lại có thể phát hiện âm thanh ở mức 30 decibel, tương tự như âm thanh thì thầm. Hai tháng sau chỉnh sửa gene, chuột Beethoven thể hiện khả năng nghe tốt hơn so với chuột mang đột biến mà không được điều trị, khả năng phát hiện âm thanh ở khoảng 45 decibel, tương đương cuộc trò chuyện bình thường.
Ngoài ra, những con chuột Beethoven và những con chuột khỏe mạnh được điều trị đều giữ lại một số lượng tế bào thính giác bình thường với cấu trúc gần như nguyên vẹn. Theo nhóm đề tài, phương pháp trên hứa hẹn cho 15 dạng điếc di truyền do nguyên nhân khác nhau gây ra, đó là đột biến chữ cái trong chuỗi ADN của các gene thính lực.