Ngày 4/11, Cục Quản lý Dược (Bộ Y tế) cho biết, vừa ra quyết định đình chỉ thuốc viên bao đường Tiêu độc PV, số lô: 03.12.14, ngày SX: 2/12/2014, HD: 21/12/2017, SĐK: V1613-H12-10, do Công ty Cổ phần dược thảo Phúc Vinh sản xuất. Nguyên nhân thuốc viên bao đường Tiêu độc PV số lô trên bị đình chỉ lưu hành và thu hồi là do kiểm nghiệm không đạt tiêu chuẩn chất lượng về chỉ tiêu định tính Thổ phục linh.
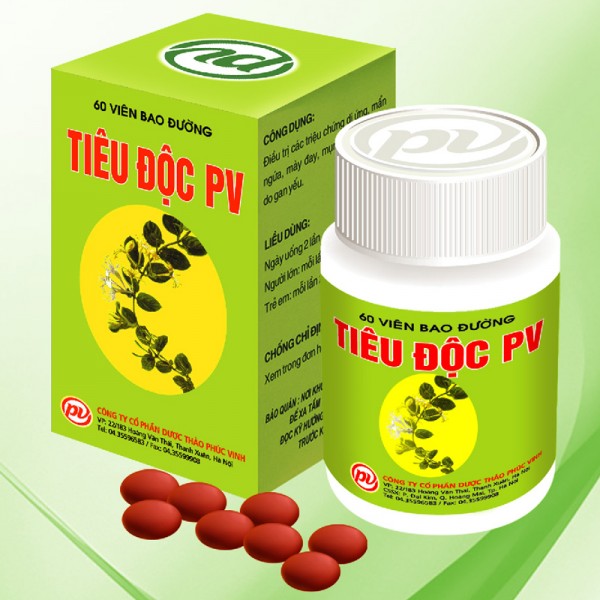 |
| Thuốc tiêu độc PV bị đình chỉ lưu hành và thu hồi (ảnh sản phẩm không thuộc lô thuốc bị thu hồi). Ảnh http://duocphucvinh.com/ |
Thuốc tiêu độc PV được quảng cáo có tác dụng chống dị ứng, giải độc, chống viêm. Thành phần của thuốc gồm một số loại dược liệu như Kim ngân hoa, Thổ phục linh 600 mg, Mã đề…
Ngoài ra, Cục Quản lý Dược cũng đình chỉ lưu hành và thu hồi thuốc viên nén Ciprofloxacin tablets USP 500mg, số lô: FCF602B, ngày SX: 03/01/2016, HD: 02/01/2019, SĐK: VN-15526-12 do Công ty Macleods Pharmaceuticals Ltd., India sản xuất. Công ty Cổ phần Tập đoàn Dược phẩm và Thương mại Sohaco nhập khẩu. Thuốc viên nén Ciprofloxacin tablets USP 500mg bị đình chỉ lưu hành và thu hồi do không đạt tiêu chuẩn chất lượng về chỉ tiêu độ hòa tan.
Thuốc viên nén Ciprofloxacin tablets USP 500mg được chỉ định dùng trong điều trị các bệnh lý nhiễm khuẩn hô hấp, tai mũi họng, thận hoặc đường niệu, sinh dục kể cả bệnh lậu, tiêu hóa, ống mật, xương khớp, mô mềm, sản phụ khoa, nhiễm trùng máu, viêm màng não, viêm phúc mạc, nhiễm trùng mắt.
Cục Quản lý Dược yêu cầu nhà sản xuất phải báo cáo việc thu hồi thuốc tiêu độc PV và thuốc viên nén Ciprofloxacin tablets USP 500mg về Cục trước ngày 7/11/2016
Cục Quản lý Dược đề nghị Sở Y tế các tỉnh thành phố, Y tế các ngành thông báo cho các cơ sở kinh doanh, sử dụng thuốc thu hồi các lô thuốc không đạt chất lượng nêu trên, kiểm tra và giám sát các đơn vị thực hiện thông báo này; xử lý những đơn vị vi phạm theo quy định hiện hành; báo cáo về Cục Quản lý Dược và các cơ quan chức năng có liên quan.
