Bộ Y tế không cập nhật kịp thời việc gia hạn vaccine Covid-19 Pfizer?

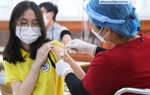
Nhân viên y tế tiêm vaccine Pfizer-BioNTech ngừa Covid-19 cho trẻ từ 12 đến 17 tuổi. Ảnh minh họa
Vaccine Ffizer-BioN/Tech ngừa Covid-19 đã được WHO gia hạn sử dụng từ tháng 8/2021. Tuy nhiên, Bộ Y tế đã không cập nhật kịp thời việc gia hạn sử dụng vaccine Pfizer-BioN/Tech khiến dư luận hiểu nhầm.
Mới đây, Bộ Y tế đã gia hạn 2 lô vaccine ngừa Covid-19 Pfizer từ 3 tháng lên 9 tháng khiến dư luận dậy sóng. Bởi lẽ, theo thông tin từ nhà sản xuất, 2 lô vaccine trên có thời hạn sử dụng 6 tháng, đến cuối tháng 11/2021. Vì vậy, dư luận cho rằng, có sự "mập mờ" của Bộ Y tế về việc nhập vaccine gần hết hạn, rồi gia hạn để tiêm cho người dân. Tuy nhiên, theo tìm hiểu của PNVN, việc tăng hạn vaccine ngừa Covid-19 Pfizer đã được các tổ chức quốc tế thông tin từ lâu. Có chăng, Bộ Y tế "không cập nhật" kịp thời dẫn đến dư luận hiểu nhầm.
Theo đó, ngày 22/8/2021, Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đã cập nhật giấy phép sử dụng khẩn cấp vaccine Pfizer-BioN/Tech để hỗ trợ việc kéo dài thời hạn sử dụng của vaccine này từ 6 tháng lên 9 tháng (tức thêm 3 tháng) trong điều kiện được bảo quản ở nhiệt độ -90 độ đến -60 độ C.
Theo FDA, việc gia hạn cũng có thể áp dụng cho các lô có thể đã hết hạn trước khi sửa đổi EUA, miễn là sản phẩm được bảo quản ở cùng nhiệt độ.
Về vấn đề trên, TS.Kidong Paark, Trưởng Đại diện Tổ chức Y tế Thế giới (WHO) tại Việt Nam, cho biết, ngày 31/12/2020, WHO đã phê duyệt vaccine Pfizer-BioNTech ngừa Covid-19 và đưa vào Danh sách Sử dụng Khẩn cấp của WHO. Đây là vaccine ngừa Covid-19 đầu tiên được WHO phê duyệt.
Ngày 8/1/2021, WHO đưa ra khuyến nghị về việc sử dụng và các yêu cầu bảo quản đối với vaccine Pfizer-BioNTech Covid-19 như sau: Vaccine dùng cho người từ 16 tuổi trở lên; 2 liều cách nhau từ 21 đến 28 ngày; Mỗi liều dung tích 0,3 ml, hàm lượng 30microgram, tiêm bắp ở cơ Delta; Bảo quản trong môi trường tủ âm sâu tới 6 tháng. Đây là những khuyến nghị dựa trên dữ liệu khoa học có được vào thời điểm đó.
Vaccine Pfizer-BioNTech ngừa Covid-19
Tuy nhiên, nhà sản xuất tiếp tục nghiên cứu và phát triển sau giai đoạn phê duyệt ban đầu. Các cơ quan quản lý vaccine quốc gia đã cập nhật các điều kiện phê duyệt sau khi xem xét các bằng chứng và dữ liệu khoa học mới do nhà sản xuất cung cấp. Cập nhật gồm có: Mở rộng nhóm tuổi tiêm từ 16 tuổi trở lên thêm nhóm từ 12 tuổi trở lên; Tăng hạn sử dụng từ 6 tháng lên 9 tháng.
Sau khi xem xét, WHO đồng ý phê duyệt gia hạn sử dụng vào tháng 8/2021. Việc gia hạn sử dụng lên 9 tháng áp dụng với tất cả các loại vaccine Pfizer được sản xuất kể từ khi được phê duyệt đầu tiên vào cuối tháng 12/2020.
Cũng theo TS.Kidong Paark, để gia tăng hạn sử dụng thêm 3 tháng thì vaccine Pfizer phải đáp ứng 3 yêu cầu. Đó là: Vaccine Pfizer-BioNTech Covid-19 có thể được bảo quản trong tủ âm sâu từ -90 đến -60 độ C với thời gian lên đến 9 tháng; Sau khi lấy ra khỏi tủ âm sâu, lọ vaccine chưa pha có thể được bảo quản tối đa 31 ngày ở nhiệt độ 2 độ C đến 8 độ C, trước khi sử dụng. Trong thời hạn sử dụng 9 tháng, các lọ chưa mở có thể được bảo quản và vận chuyển ở -25 độ C đến -15 độ C trong thời gian tối đa 2 tuần.
TS.Kidong Paark cũng cho biết, việc gia tăng hạn sử dụng vaccine thêm 3 tháng vẫn đảm bảo chất lượng, an toàn và hiệu quả phòng chống Covid-19. Dữ liệu từ nghiên cứu tính ổn định đã chứng minh rằng, chất lượng của vaccine đáp ứng các yêu cầu sử dụng. Do đó, chất lượng vaccine là như nhau đến 9 tháng.
Đối với Việt Nam, về việc sử dụng vaccine Pfizer với hạn sử dụng gia tăng không ảnh hưởng đến hiệu quả phòng Covid-19, miễn là vaccine còn trong hạn sử dụng và được bảo quản trong các điều kiện đạt yêu cầu. Ngoài ra, những vaccine này có thể được sử dụng để tiêm chủng cho cho nhóm đối tượng đã được phê duyệt sử dụng. Đối với vaccine Pfizer-BioNTech Covid-19, nhóm đối tượng được WHO cấp phép sử dụng là nhóm người từ 12 tuổi trở lên.
Trước đó, ngày 30/11, Vệ sinh dịch tễ TƯ (Bộ Y tế) đã có văn bản hỏa tốc số 2738 thông báo đến Trung tâm Kiểm soát dịch bệnh (CDC) các tỉnh/thành về việc tăng thời hạn sử dụng của vaccine Pfizer nhập khẩu (gồm 2 lô là 124001 và 123002) để triển khai tiêm cho trẻ em từ 12 đến 17 tuổi.
Theo đó, sẽ áp dụng hạn dùng mới là 9 tháng đối với các lô vaccine có hạn dùng 6 tháng in trên nhãn (tăng 3 tháng hạn dùng so với hạn dùng in trên nhãn). Do đó, Viện Vệ sinh dịch tễ TƯ đề nghị CDC các địa phương thông báo đến các đơn vị, điểm tiêm chủng trên địa bàn áp dụng hạn dùng của 2 lô vaccine 24001 và 123002 là ngày 28/2/2022.
Trước đó, ngày 20/9 và 6/10, Cục Quản lý Dược (Bộ Y tế) nhận được các văn bản của Công ty TNHH Pfizer (Việt Nam) về việc đề nghị tăng hạn dùng của vaccine Comirnaty (vaccine Pfizer) từ 6 tháng lên 9 tháng ở điều kiện bảo quản -90 độ C đến -60 độ C. Đến ngày 22/10, Cục Quản lý Dược có văn bản gửi Công ty TNHH Pfizer đồng ý về việc tăng hạn dùng ở điều kiện bảo quản -90 độ C đến -60 độ C của vaccine Cominaty (đã được Bộ Y tế phê duyệt có điều kiện cho nhu cầu cấp bách trong phòng, chống dịch bệnh Covid-19) từ 6 tháng lên 9 tháng.
Văn bản này nêu rõ, căn cứ kết luận của Hội đồng tư vấn cấp Giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc và thực hiện ý kiến chỉ đạo của lãnh đạo Bộ, Cục Quản lý dược đồng ý về việc tăng hạn dùng của vaccine Pfizer từ 6 tháng lên 9 tháng. "Công ty TNHH Pfizer Việt Nam phải chịu trách nhiệm về chất lượng đối với vaccine lưu hành trên thị trường và có trách nhiệm thông báo sự thay đổi này đến các đơn vị liên quan", văn bản yêu cầu.
* Bài tuyên truyền thực hiện Nghị quyết 84/NQ-CP ngày 29/5/2020 của Chính phủ