Bộ Y tế phân bổ 54.000 lọ thuốc Remdesivir điều trị Covid-19
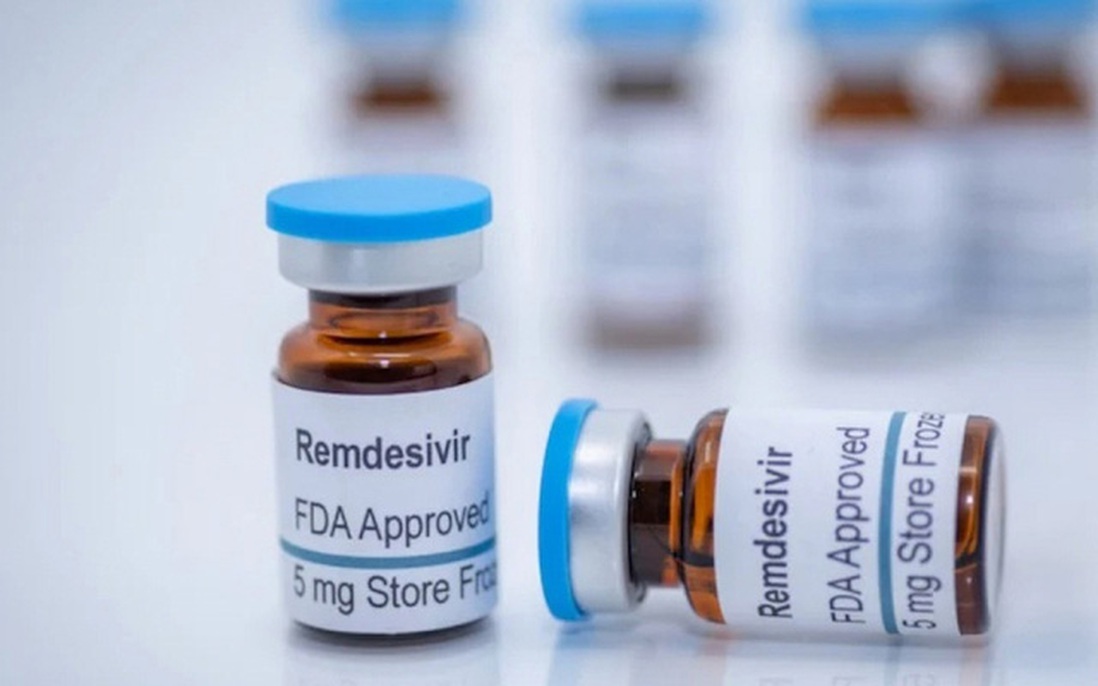
Thuốc Remdesivir điều trị Covid-19
Sau khi tiếp nhận 54.000 lọ thuốc Remdesivir, Bộ Y tế đã phân bổ cho các cơ sở điều trị Covid-19, chủ yếu là ở TP. Hồ Chí Minh. Tổng cộng, đến nay Bộ Y tế đã phân bổ 227.680 lọ thuốc Remdesivir phục vụ công tác điều trị Covid-19.
Ngày 3/9, Bộ Y tế cho biết, sau khi tiếp nhận 54.000 lọ thuốc Remdesivir điều trị Covid-19, Bộ đã phân bổ cho các cơ sở điều trị Covid-19. Đây là lần phân bổ thứ 5 của Bộ Y tế, tập trung chủ yếu cho các cơ sở điều trị Covid-19 trên địa bàn TP. Hồ Chí Minh.
Như vậy, đến nay Bộ Y tế đã phân bổ 227.680 lọ thuốc Remdesivir phục vụ công tác điều trị Covid-19. Trước đó, Bộ Y tế cũng đã phân bổ 4 đợt thuốc Remdesivir với khoảng 173.680 lọ cho các cơ sở điều trị bệnh nhân Covid-19 trên địa bàn TP. Hồ Chí Minh và cơ sở điều trị Covid-19 trên cả nước.
Theo Bộ Y tế, số thuốc Remdesivir đã phân bổ nằm trong số 500.000 lọ do Tập đoàn Vingroup đã đàm phán mua và tặng Bộ Y tế phục vụ điều trị bệnh nhân Covid-19.
Theo hướng dẫn của Bộ Y tế, thuốc này ưu tiên sử dụng cho nhóm nguy cơ cao gồm người trên 65 tuổi, người có bệnh nền, béo phì (BMI >25). Bộ Y tế lưu ý không bắt đầu sử dụng thuốc cho người bệnh Covid-19 cần thở máy xâm nhập, ECMO (tim phổi nhân tạo). Riêng đối với các trường hợp được điều trị bằng thuốc Remdesivir trước khi thở máy xâm nhập hoặc ECMO thì tiếp tục dùng thuốc Remdesivir cho đủ liệu trình.
Được biết, Remdesivir là thuốc kháng virus, được Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) phê duyệt khẩn cấp để điều trị cho bệnh nhân Covid-19. Remdesivir đã được 50 quốc gia như Mỹ, EU, Úc, Nhật Bản, Singapore, Ấn Độ... đưa vào phác đồ điều trị từ tháng 5/2020, và là một trong những loại thuốc đặc trị khó tiếp cận hàng đầu thế giới.
Thuốc Remdesivir cũng là thuốc đã được cấp phép khẩn cấp tại Ấn Độ, được chỉ định điều trị Covid-19, cho bệnh nhân Covid nặng, thở máy/ECMO.