Chính thức nhận đăng ký tiêm kháng thể đơn dòng Evusheld
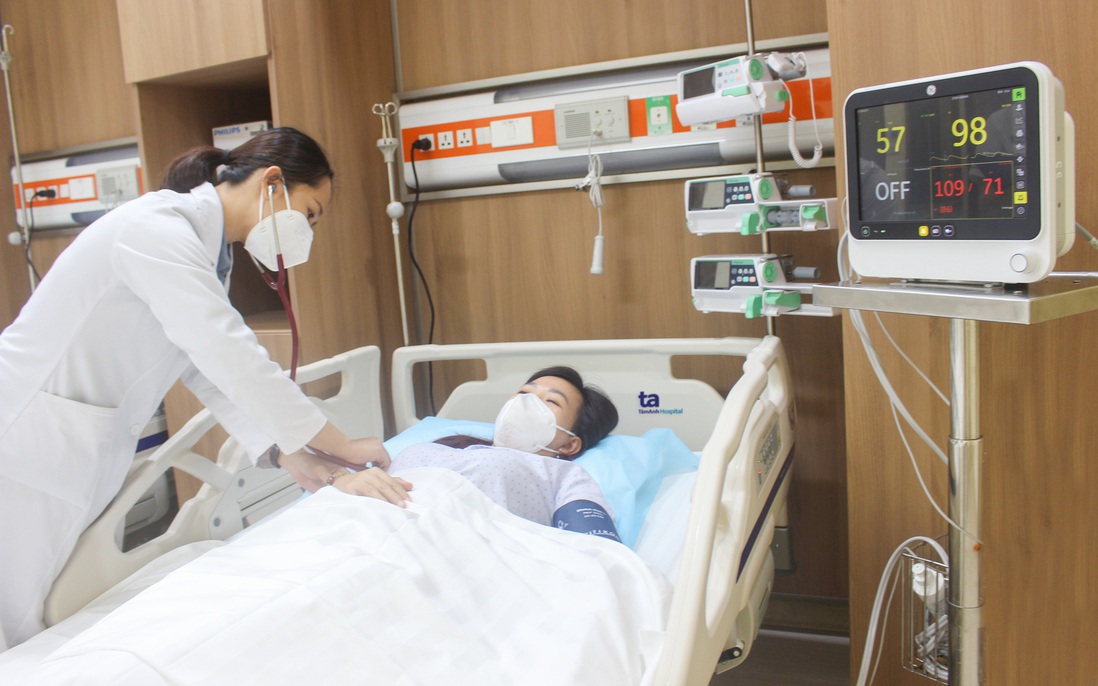
Các y bác sĩ kiểm tra sức khỏe cho đối tượng yếu thế
Evusheld là kháng thể đơn dòng được nghiên cứu và sản xuất bởi hãng dược phẩm AstraZeneca (Vương quốc Anh - Thụy Điển.
Tổ chức Y tế thế giới (WHO) ước tính khoảng 2% dân số toàn cầu thuộc nhóm dễ bị tổn thương trước Covid-19 do bị suy giảm miễn dịch vừa và nặng như HIV, ung thư, ghép tạng (ghép tim, ghép gan, ghép thận), dùng corticoid liều cao, kéo dài... Tại Việt Nam, theo thống kê của Bộ Y tế, cả nước hiện có gần 230.000 người nhiễm HIV; 6.100 ca ghép tạng và hàng trăm ngàn trường hợp mắc ung thư mới mỗi năm.

Các y bác sĩ kiểm tra sức khỏe cho đối tượng yếu thế
Hiện nay, kháng thể đơn dòng Evusheld đã được cấp phép lưu hành trong tình trạng khẩn cấp tại một số quốc gia như: Mỹ, Pháp, Các tiểu vương quốc Ả Rập thống nhất, Bahrain…Tại Việt Nam, ngày 2/3/2022, Bộ đã cấp Giấy phép nhập khẩu thuốc EVUSHELD đáp ứng nhu cầu điều trị đặc biệt của cơ sở khám chữa bệnh.
Để đăng ký tiêm kháng thể đơn dòng Evusheld, người dân đăng ký tại link: https://tamanhhospital.vn/dang-ky-tiem-evusheld
Theo đánh giá, kháng thể đơn dòng Evusheld được cấp phép về Việt Nam vào thời điểm này mang ý nghĩa nhân văn sâu sắc. Bởi nhóm người yếu thế đang cần thêm một lá chắn để bảo vệ sức khỏe trước các biến thể SARS-CoV-2 đang lan rộng trong khi khó có thể đáp ứng miễn dịch tốt, mặc dù đã được tiêm đủ liều vaccine, thậm chí cả liều tăng cường.
Các chuyên gia cũng cho biết, kháng thể đơn dòng Evusheld không thay thế vaccine phòng Covid-19 cho cộng đồng, mà chỉ hướng tới những người suy giảm miễn dịch hoặc không có khả năng đáp ứng miễn dịch thỏa đáng; hoặc không sinh đầy đủ kháng thể sau khi đã tiêm đủ liều vắc xin và cho người không thể tiêm vaccine do từng xảy ra phản ứng bất lợi nghiêm trọng với vaccine Covid-19.